Phenylquecksilberacetat
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
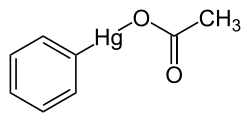
| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Phenylquecksilberacetat | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C8H8HgO2 | |||||||||||||||||||||
| Kurzbeschreibung |
beiger geruchloser Feststoff[2] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 336,74 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest[2] | |||||||||||||||||||||
| Dichte |
2,4 g·cm−3[3] | |||||||||||||||||||||
| Löslichkeit | ||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Phenylquecksilberacetat ist eine chemische Verbindung aus der Gruppe der quecksilberorganischen Verbindungen.
Gewinnung und Darstellung
Phenylquecksilberacetat kann durch Reaktion von Quecksilber(II)-oxid mit Benzol und Eisessig unter Bortrifluorid-Katalyse gewonnen werden.[5]
Eigenschaften
Phenylquecksilberacetat ist ein brennbarer, schwer entzündbarer, kristalliner, beiger, geruchloser Feststoff, der schwer löslich in Wasser ist. Er zersetzt sich bei Erhitzung über 147–150 °C.[2]
Der C–Hg–O-Bindungswinkel beträgt laut quantenmechanischen Berechnungen rund 174°, ist also fast linear.[6]
Verwendung
Phenylquecksilberacetat dient als Konservierungsmittel für Farbkonserven,[3] kosmetische Mittel und Arzneimittel. Kosmetisch ist es in der EU nur in am Auge anzuwendenden Mitteln – in Konzentrationen bis 0,007 % Quecksilber, allein oder in Kombination mit anderen zugelassenen Quecksilberverbindungen – zur Konservierung zulässig,[7] auch in anderen Ländern ist die kosmetische Verwendung beschränkt.[8] Die Verwendung als Haut- und Wunddesinfektionsmittel (z. B. Merfen-Orange N) ist nicht mehr gebräuchlich.[9] Die Verwendung in vaginalen Gels oder Schäumen als Spermizid ist heute obsolet.[10][11] Es wirkt als Katalysator in Polyurethansystemen. Es wird auch als Katalysator in den flexiblen Polyurethan-Böden der Marke 3M Tartan verwendet, die in Schulsporthallen üblich waren. Es wirkt als Antitranspirant, wenn es auf die Blätter der Pflanzen aufgetragen wird.[3] Phenylquecksilberacetat wurde als Quecksilberbeize zum Beizen von Saatgut verwendet.
Einzelnachweise
- ↑ Eintrag zu PHENYL MERCURIC ACETATE in der CosIng-Datenbank der EU-Kommission, abgerufen am 2. Oktober 2020.
- ↑ a b c d e f g Eintrag zu Phenylquecksilberacetat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 10. Januar 2025. (JavaScript erforderlich)
- ↑ a b c d Datenblatt Phenylmercury acetate, 98% bei Alfa Aesar, abgerufen am 24. September 2020 (Seite nicht mehr abrufbar).
- ↑ Eintrag zu Phenylmercury acetate in der Datenbank ECHA CHEM der Europäischen Chemikalienagentur (ECHA), abgerufen am 24. September 2020. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Franz v. Bruchhausen, Gerd Dannhardt, Siegfried Ebel, August-Wilhelm Frahm, Eberhard Hackenthal, Ulrike Holzgrabe: Hagers Handbuch der Pharmazeutischen Praxis. Springer-Verlag, 2013, ISBN 978-3-642-57880-9, S. 178 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Yizhen Tang, Claus Jørgen Nielsen: Theoretical studies of Phenylmercury carboxylates – Complexation Constants and Gas Phase Photo-Oxidation of Phenylmercurycarboxylates. Miljødirektoratet, 2010, abgerufen am 11. Dezember 2022 (englisch, Table 2.1).
- ↑ Verordnung (EG) Nr. 1223/2009 des Europäischen Parlaments und des Rates vom 30. November 2009 über kosmetische Mittel, Anhang V – Liste der in kosmetischen Mitteln zugelassenen Konservierungsstoffe. ec.europa.eu, abgerufen am 2. Oktober 2020.
- ↑ Phenylmercuric Acetate. In: R. C.Rowe (Hrsg.): Handbook of Pharmaceutical Excipients, Pharmaceutical Press, 6. Auflage, 2009. S. 492 ff.
- ↑ J. Borsch: Es war einmal ….Locabiosol & Co. In: Deutsche Apothekerzeitung, 2. Januar 2017.
- ↑ L. Lohr: Mercury controversy heats up. In: American Journal of Pharmaceutics, Band 18 (1978), S. 23.
- ↑ S. Shapiro et al.: Birth Defects and Vaginal Spermicides. In: Journal of the American Medical Association, Band 247 (1982), S. 2381–2384. doi:10.1001/jama.1982.03320420031027.